Danh sách 5 thuốc gồm: Pharcavir,êmthuốcnộinhậngiấyđăngkýlưuhàkq quan vot Zacutas 60, Zacutas 90, Dactasvir 30mg, Dactasvir 60mg, lần lượt có số đăng ký từ VD3-29-19 đến VD3-34-19.
Cục quản lý Dược yêu cầu cơ sở sản xuất và cơ sở đăng ký thuốc có trách nhiệm sản xuất thuốc theo đúng các hồ sơ, tài liệu đã đăng ký với Bộ Y tế và phải in số đăng ký được Bộ Y tế Việt Nam cấp lên nhãn thuốc.
Đồng thời thực hiện việc cập nhật tiêu chuẩn chất lượng của thuốc theo quy định. Cập nhật nhãn thuốc, tờ hướng dẫn sử dụng thuốc theo quy định tại Thông tư số 01/2018 trong thời hạn 6 tháng kể từ ngày ký ban hành Quyết định này, theo hình thức thay đổi, bổ sung giấy đăng ký lưu hành thuốc quy định tại Thông tư số 32/2018/TT-BYT ngày 12/11/2018 của Bộ trưởng Bộ Y tế quy định việc đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
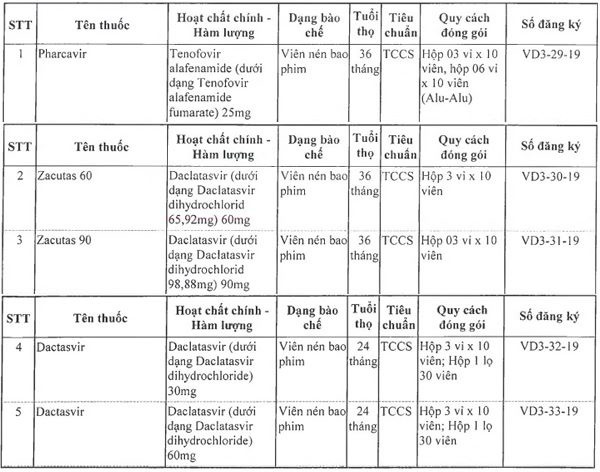 |
| Danh sách 5 thuốc mới được cấp giấy đăng lý lưu hành |
Đối với thuốc Pharcavir chứa hoạt chất tenofovir alafenamide fumarate (thuốc số 1 tại danh mục) phải cập nhật tờ hướng dẫn sử dụng theo tờ hướng dẫn sử dụng thuốc Vemlidy đã được Cơ quan Quản lý Dược Châu Âu (EMA) phê duyệt trong thời hạn 03 tháng kể từ ngày ký ban hành Quyết định này và chỉ được sản xuất, lưu hành sau khi được Cục Quản lý Dược phê duyệt nội dung này.
Các có sở sản xuất cần phối hợp với các cơ sở điều trị để thực hiện theo đúng các quy định hiện hành về thuốc kê đơn, theo dõi an toàn, hiệu quả, tác dụng không mong muốn của thuốc trên người Việt Nam.
Cơ sở đăng ký thuốc phải bảo đảm duy trì điều kiện hoạt động trong thời gian hiệu lực của giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc. Trong trường hợp không còn đáp ứng đủ điều kiện hoạt động, cơ sở đăng ký phải có trách nhiệm thực hiện thay đổi cơ sở đăng ký.
Đối với thuốc số thứ tự 02, 03, 04, 05 (chứa hoạt chất daclatasvir dihydrochlorid) tại Danh mục ban hành kèm theo Quyết định này, cơ sở phải gửi mẫu thuốc kèm theo chất chuẩn đối với 03 lô sản xuất đầu tiên để Viện Kiểm nghiệm thuốc Trung ương hoặc Viện Kiểm nghiệm thuốc TP.HCM kiểm tra theo tiêu chuẩn chất lượng đã đăng ký, chỉ được lưu hành sau khi kết quả kiểm nghiệm đạt yêu cầu.
T.Thư


 相关文章
相关文章


 精彩导读
精彩导读



 热门资讯
热门资讯 关注我们
关注我们
